L’hyperkaliémie a une prévalence élevée chez les patients présentant une insuffisance rénale1 et elle peut compromettre les effets bénéfiques du traitement par inhibiteurs du SRAA2,3
Help us guide you to the right place
I reside in the United States
Visit the US site
Help us guide you to the right place
I am practicing from:

Austria
-

Austria
-

Belgium
-

Germany
-

Ireland
-

Italy
-

Netherlands
-

Portugal
-

Spain
-

Switzerland
-
Other
Help us guide you to the right place
I am residing in:

Austria
-

Austria
-

Belgium
-

Germany
-

Ireland
-

Italy
-

Netherlands
-

Portugal
-

Spain
-

Switzerland
-
Other

Bitte verwenden Sie als Benutzernamen die E-Mail Adresse, welche Sie bei der Registration angegeben hatten. Falls Sie das Passwort vergessen haben, können Sie sich einen Reaktivierungslink zustellen lassen. Alternativ ist für bereits registrierte Health Professionals auch eine Anmeldung mit der HPC-Card von FMH oder pharmaSuisse möglich.
please proceed.
HYPERKALIÉMIE EN CAS D’IRC
Déclarer les évènements indésirables:
Les évènements indésirables doivent être déclarés au groupe CSL Vifor.
pv.vif@viforpharma.com
LE TRAITEMENT PAR INHIBITEURS DU SRAA EST VITAL
La progression de l’IRC vers une insuffisance rénale terminale, l’absence de dialyse ou la mise en attente de son commencement, ainsi que les risques associés à celle-ci sont des facteurs d’une importance capitale pour les patients.4
- Concernant le ralentissement du déclin de la fonction rénale et la diminution de la protéinurie, il a été montré que les inhibiteurs du SRAA étaient plus efficaces que les autres antihypertenseurs.4-6
Les inhibiteurs du SRAA constituent le fondement du traitement de l’IRC. Leur utilisation à la dose tolérée la plus élevée est recommandée par plusieurs organismes4,7
- Deux essais de référence (IDNT8: Irbesartan Diabetic Nephropathy Trial et RENAAL9: Reduction of Endpoints in NIDDM with the Angiotensin II Antagonist Losartan) ont été mené chez des patients présentant un diabète de type 2 et une IRC, ainsi qu’une albuminurie >1 g/j.
- L’effet néphroprotecteur de ces médicaments a été mis en évidence par une diminution de 16 à 20% du critère d’évaluation combiné comprenant le risque de décès, la progression vers une dialyse ou le doublement de la créatinine sérique.4,8,9
- L’utilisation de ramipril chez les patients ayant une néphropathie non diabétique a également eu un effet néphroprotecteur en diminuant à la fois la protéinurie et la vitesse du déclin du DFG.10
IDNT et RENAAL: diminution du risque de décès, d'IRC terminale et de doublement de la concentration de créatinine sérique avec les inhibiteurs du SRAA8,9
IDNT8
Population de patients:
1,715
Patients atteints de néphropathie diabétique
Traitement:
Une fois par jour, 300 mg d’irbésartan, 10 mg d’amlodipine ou placebo
Critère d’évaluation principal:
Composite: décès, IRC terminale ou doublement
de la créatinine sérique initiale
Suivi médian:
2.6
ans
Diminution du risque du critère d’évaluation principal:
20%
vs placebo
(p=0.02)
23%
vs amlodipine
(p=0.006)
RENAAL9
Population de patients:
1,513
Patients atteints de néphropathie diabétique
Traitement
Une fois par jour, losartan 50−100 mg ou placebo
Critère d’évaluation principal:
Composite: décès, IRC terminale ou doublement
de la créatinine sérique initiale
Suivi médian:
3.4
ans
Diminution du risque du critère d’évaluation principal:
16%
vs placebo
(p=0.02)
LE RISQUE D’HYPERKALIÉMIE EST EXACERBÉ PAR LES INHIBITEURS DU SRAA
L’utilisation des inhibiteurs du SRAA recommandés par les directives a été citée comme l’un des facteurs principaux d’apparition d’une hyperkaliémie chez les patients atteints d’IRC.11
- Les essais cliniques ont montré que les inhibiteurs du SRAA augmentaient le risque d’hyperkaliémie chez les patients atteints d’IRC.12
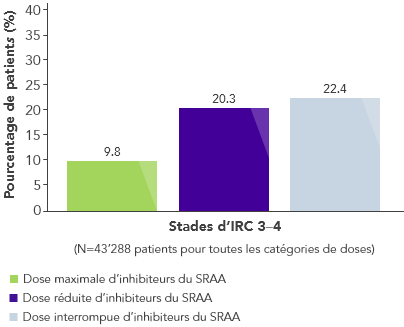
- Selon des études concrètes concordantes, le risque d’hyperkaliémie est multiplié par 1,5 chez les patients sous inhibiteurs du SRAA13,14. Plus la néphropathie est grave, plus le risque est élevé.15
Lors de la première année de traitement par inhibiteurs du SRAA, plus la néphropathie était grave plus le pourcentage de patients atteints d’hyperkaliémie était élevé15
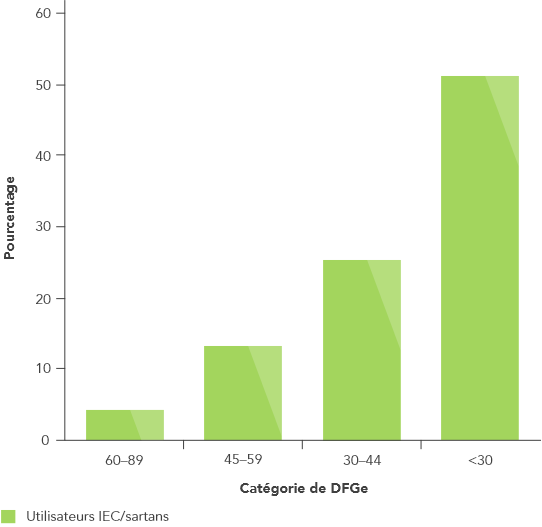

Impact des inhibiteurs du SRAA sur le système rénine-angiotensine-aldostérone
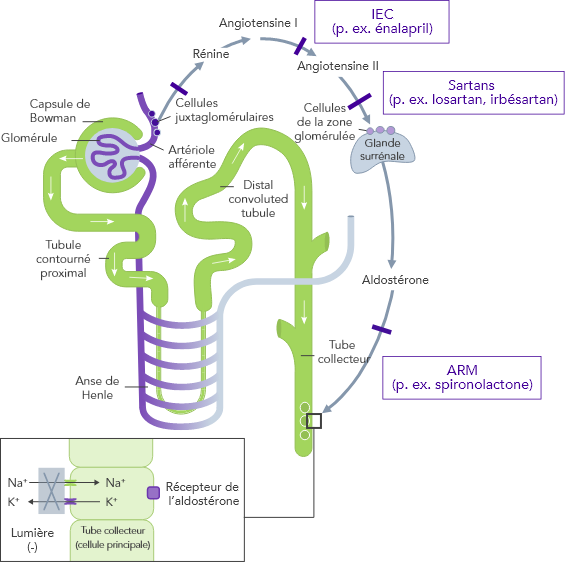

D’HYPERKALIÉMIE


SYSTÈME RÉNINE–ANGIOTENSINE–
ALDOSTÉRONE


L’HYPERKALIÉMIE MÈNE À UNE UTILISATION SOUS-OPTIMALE DES INHIBITEURS DU SRAA
Les lignes directrices actuelles recommandent de diminuer la dose des inhibiteurs du SRAA ou d’interrompre leur prise en cas d’hyperkaliémie persistante posant problème chez les patients atteints d’IRC. Par conséquent, l’hyperkaliémie est l’une des principales raisons de l’arrêt du traitement par inhibiteurs du SRAA.2,3
- Dans une grande analyse de base de données des États-Unis,2 ~40% et ~50% des patients prenant la dose maximale d’inhibiteurs du SRAA, et présentant respectivement une hyperkaliémie légère ou modérée à sévère, ont dû diminuer leur dose ou arrêter leur traitement après un événement d’hyperkaliémie.
Le traitement est diminué ou arrêté chez près de la moitié des patients prenant la dose maximale d’ inhibiteurs du SRAA après un événement d’hyperkaliémie2
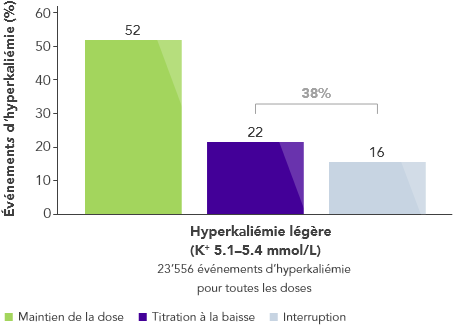


Le traitement est diminué ou arrêté chez près de la moitié des patients prenant la dose maximale d’ inhibiteurs du SRAA après un événement d’hyperkaliémie2
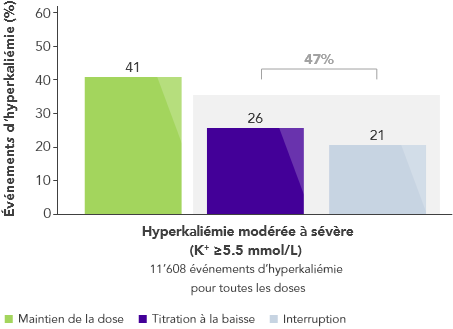


LÉGÈRE


À SÉVÈRE


Toutefois, la diminution ou l’arrêt des inhibiteurs du SRAA sont associés à une augmentation du risque de mortalité et de morbidité.2,16
![]()
Ainsi, les médecins font souvent face à un dilemme: utiliser des inhibiteurs du SRAA et accepter l’hyperkaliémie ou réduire/arrêter les inhibiteurs du SRAA et accepter des résultats cliniques plus mauvais
Ce qu’il faut, c’est un traitement qui permettrait aux patients atteints d’IRC de continuer de bénéficier du traitement par inhibiteurs du SRAA tout en maintenant un contrôle à long terme fiable du K+ sérique.
Le risque de mortalité double quand les inhibiteurs du SRAA sont diminués ou arrêtés2
LES POSSIBILITÉS THÉRAPEUTIQUES ACTUELLES DE L’HYPERKALIÉMIE CHRONIQUE SONT LIMITÉES
Les stratégies thérapeutiques à court et à long terme sont essentielles à la prise en charge de l’hyperkaliémie.17 Toutefois, les possibilités actuellement disponibles sont principalement axées sur les soins courants et d’urgence,17 et les possibilités thérapeutiques actuelles de l’hyperkaliémie chronique sont très restreintes:
Les modifications alimentaires peuvent limiter la consommation d’aliments sains,18. De plus, pour les patients suivant déjà un régime restrictif, il peut être très difficile de respecter des modifications alimentaires supplémentaires.19,20 Les effets des interventions alimentaires sur les résultats sont incertains.19
Les diurétiques de l’anse non épargneurs de K+ dépendent de la fonction rénale résiduelle et sont associés à un risque accru de goutte et de diabète, à une contraction du volume, à une moindre excrétion du K+ et à une sarcopénie.17,21
Les substances se liant habituellement au K+ (polystyrène sulfonate sodique et polystyrène sulfonate calcique) peuvent être associées à des effets secondaires GI menaçant le pronostic vital et à une hypokaliémie22,23 et peuvent ne pas convenir aux personnes incapables de tolérer une augmentation du Na+ (polystyrène sulfonate sodique).23

Jusqu'à récemment, il n'existait pas de possibilité fiable à long terme de prise en charge de l’hyperkaliémie chronique, permettant aux patients de continuer le traitement par inhibiteurs du SRAA aux doses cibles.17
Ca2+: ions calcium; IRC: insuffisance rénale chronique; CV: cardiovasculaire; HK: hyperkaliémie; K+: ions potassium; Na+: ions sodium; SRAA: système rénine-angiotensine-aldostérone.
Notes de bas de page:
Veltassa® est indiqué dans le traitement de l’hyperkaliémie chez l’adulte.7
Références:
1. Weir MR, et al. N Engl J Med 2015;372(3):211–21. 2. Bakris GL, et al. JAMA 2015;314(2):151–61. 3. Bushinsky DA, et al. Kidney Int 2015;88:1427–33. 4. Pitt B, et al. Eur Heart J 2011;32:820–8. 5. Agarwal R, et al. Lancet 2019;394(10208):1540−50. 6. Li L, et al. J Card Pharmacol Ther 2016;21(5):456–65. 7. Information professionnelle Veltassa®: www.swissmedicinfo.ch 8. Di Lullo L, et al. Cardiorenal Med 2019;9(1):8−21. 9. Rastegar A, Soleimani M. Postgrad Med J 2001;77(914):759−64. 10. Kjeldsen KP, Schmidt TA. Eur Heart J 2019;21(Suppl A):A2−A5. 11. Collins AJ, et al. Am J Nephrol 2017;46(3):213−21. 12. Kovesdy CP, et al. Eur Heart J 2018;39(17):1535−42. 13. Rossignol P, et al. Clin Kidney J 2020;13:714−9. 14. Palmer BF, et al. N Engl J Med 2004;351:585–92. 15. KDIGO Clinical Practice Guideline for Diabetes Management in Chronic Kidney Disease. Kidney Int 2020;98(Suppl 4S):S1–S116. 16. KDIGO Clinical Practice Guideline for the Evaluation and Management of Chronic Kidney Disease. Kidney Int Suppl 2013;3:1–150. 17. National Kidney Foundation. K/DOQI Clinical Practice Guidelines on Hypertension and Antihypertensive Agents in Chronic Kidney Disease. 2004. Available at: kidneyfoundation.cachefly.net/professionals/KDOQI/guidelines_bp/index.htm (accessed July 2020). 18. Heart Outcomes Prevention Evaluation Study Investigators. Lancet 2000;355(9200):253−9. 19. SOLVD Investigators. N Engl J Med 1991;325(5):293−302. 20. Desai AS, et al. J Am Coll Cardiol 2007;50(20):1959−66. 21. Pitt B, et al. N Engl J Med 1999;341(10):709−17. 22. Zannad F, et al. N Engl J Med 2011;364:11–21. 23. McMurray JJ, et al. N Engl J Med 2014;371(11):993−1004. 24. Solomon SD, et al. N Engl J Med 2019;381(17):1609−20. 25. Epstein M, et al. Am J Manag Care 2015;21(11 Suppl):S212−S220. 26. Kovesdy CP, et al. Postgrad Med 2020;132:176–83. *Les données sont basées sur la pratique.

